保证催化剂结构在反应过程中的稳定是衡量催化剂活性的基本前提。甘油氢解反应通常在 160~220 ℃和一定的 H 2 压力下进行。 选择水作为甘油氢解反应的溶剂时,反应条件下形成的水热环境对催化剂的稳定性提出了苛刻的要求。例如,金属 Cu 粒子很容易在反应过程中发生聚集 [23] 。 Bienholz 等 [24] 在近期发现使用非水溶剂能够有效避免以上问题。
实际上,在二氧六环 [6] 、环丁砜 [6] 及醇类 [24] 等极性有机溶剂中,甘油氢解反应同样可以有效地进行。在这里,二氧六环被选为甘油氢解反应的溶剂,一方面用来保持催化剂结构在反应过程中的稳定,另一方面可以尽量减小MgO-Al 2 O 3 复合氧化物通过改变溶液 pH 值而对甘油氢解反应活性带来的影响。我们首先考察了载体组成对Cu/MgO-Al 2 O 3 催化剂甘油氢解活性的影响(表 3)。
在约 25%的甘油转化率下,4 wt% Cu/Al 2 O 3 催化剂具有很低的甘油氢解活性,其对应的甘油转化速率仅为 0。1 mol/mol surface Cu-s。在载体中引入 MgO 组分后, 催化剂的活性显著提高。 4 wt%Cu/MgO-Al 2 O 3 (1/1)催化剂的甘油转化速率为 1。6mol/mol surface Cu-s,是 4 wt% Cu/Al 2 O 3 催化剂的活性的 16 倍。进一步增加载体中的 MgO 含量, Cu/MgO-Al 2 O 3 催化剂的甘油氢解活性也随之提高。在所研究的5 个催化剂中, 4 wt% Cu/MgO 表现出甘油的转化速率(2。4 mol/mol surface Cu-s)。尽管以上催化剂的甘油氢解活性随载体的组成发生显著变化,但是它们对甘油氢解反应的选择性基本相同。 1,2-丙二醇是反应的主产物,选择性介于90%~94%,其对应的主要副产物为乙二醇,选择性保持在 5%~8%。该结果与在水溶液中铜基催化剂对甘油氢解反应的选择性相似。这暗示将二氧六环代替水作为溶剂并没有改变甘油氢解反应的路径,甘油在金属 Cu 催化剂表面脱氢生成甘油醛仍是反应的决速步骤。
考虑到以上催化剂中 Cu 粒子的本征脱氢活性非常接近,同时载体表面碱性位密度随MgO-Al 2 O 3 复合氧化物中 Mg/Al 比例的提高而增大(表 1),催化剂氢解活性随载体中MgO含量的变化应源自MgO上的碱性中心对甘油脱氢过程的助催化作用。
此外,在使用 4 wt%Cu/Al 2 O 3 催化剂时额外机械混合一定量的 MgO-Al 2 O 3(3/1)复合氧化物并没有改变原有催化剂的活性和选择性,表明在 Cu/MgO-Al 2 O 3 催化剂中碱性中心通过协同作用直接促进了金属 Cu 的甘油氢解活性,而非通过改变反应体系的 OH- 浓度来间接影响甘油的转化速率。
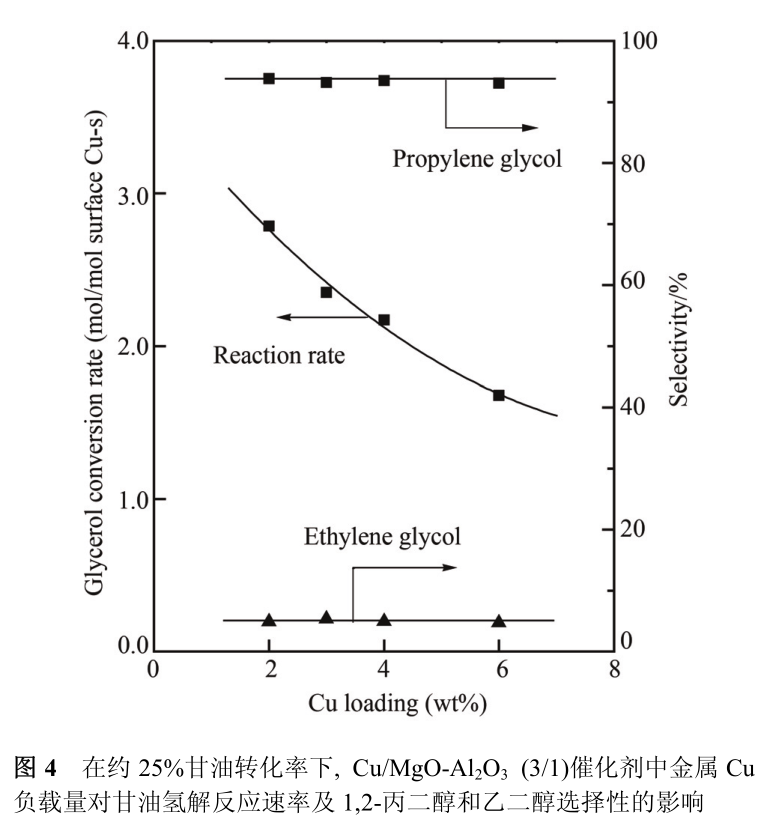
为了进一步证实 Cu/MgO-Al 2 O 3 催化剂中碱性中心与金属中心存在协同效应,我们考察了金属 Cu 负载量对 Cu/MgO-Al 2 O 3 (3/1)催化剂甘油氢解活性的影响。如图4所示,在约25%的甘油转化率下, 随Cu/MgO-Al 2 O 3(3/1)催化剂中Cu 负载量从2 wt%增长到6 wt%,甘油的转化速率从 2。8 mol/mol surface Cu-s 下降至 1。7 mol/molsurface Cu-s,而 1,2-丙二醇和乙二醇的选择性则没有明显变化。由于催化剂中 Cu 粒子的本征脱氢活性并没有随金属Cu的负载量发生改变,增加金属Cu负载量使催化剂单位表面 Cu 原子活性下降的原因可归结于催化剂表面 Cu 原子可及碱性位点数目的减少。
因此,分别调变 Cu/MgO-Al 2 O 3 催化剂中碱性中心密度和金属中心密度的两组实验均证实在甘油氢解反应中 Cu/MgO-Al 2 O 3催化剂上的碱性中心跟金属中心协同完成甘油脱氢为甘油醛。碱性中心和金属中心之间的协同作用可以通过Cu/MgO-Al 2 O 3 催化剂表面碱性位与Cu原子的比例进行定量描述。
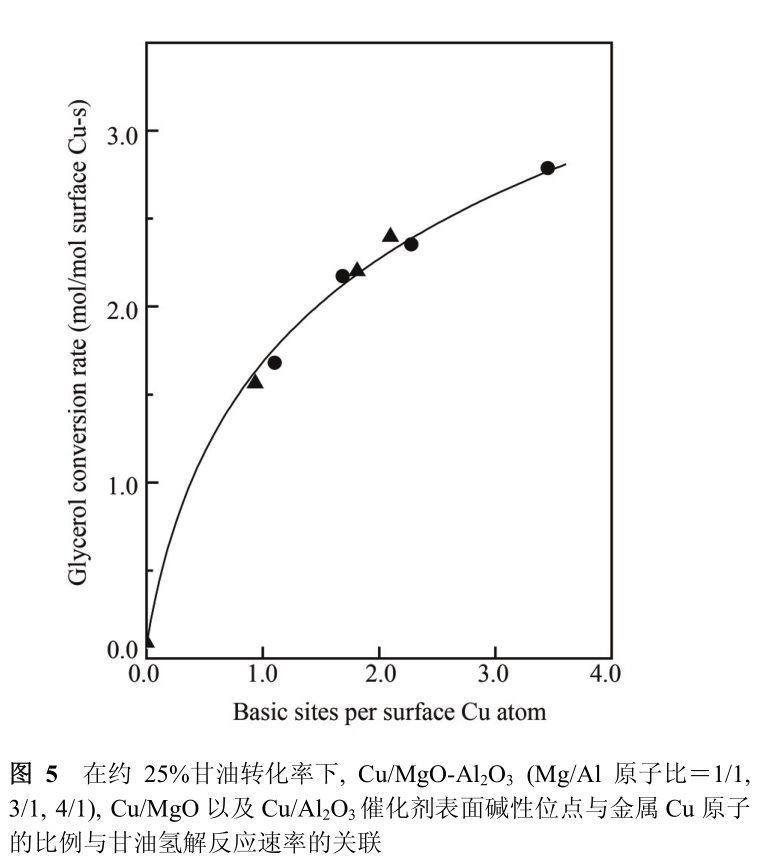
综合以上淮安化工厂家两组实验结果于图 5 中,可以看到Cu/MgO-Al 2 O 3 催化剂的甘油氢解活性随催化剂表面碱性位与 Cu 原子比例的增加而增加,两者具有很好的相关性。值得注意的是, Cu/MgO-Al 2 O 3 催化剂的甘油氢解活性随催化剂表面碱性位与 Cu 原子比例的增长趋势在催化剂表面具有高的碱性位与 Cu 原子比例时变缓。
这暗示当催化剂表面的 Cu 粒子周围具有充分的可及碱性位时,催化剂的甘油氢解活性主要取决于 Cu 粒子本身的脱氢能力。图 5 中 Cu/MgO-Al 2 O 3 催化剂的甘油氢解活性与催化剂表面碱性位与金属 Cu 原子的比例良好相关性暗示不同 Mg/Al 比例的 Cu/MgO-Al 2 O 3 催化剂表面具有相同的碱性位点,即源自与 Mg 2+ 键连的 O 2 - 离子。考虑到反应体系中原本残留的少量水以及在甘油氢解反应过程中生成的水均会使 MgO-Al 2 O 3 载体的表面发生羟基化 [25,26] 。
因此,随甘油氢解反应的进行, Cu/MgO-Al 2 O 3催化剂表面的碱性位点会从 O 2- 离子向羟基(B 碱 OH - )转变。
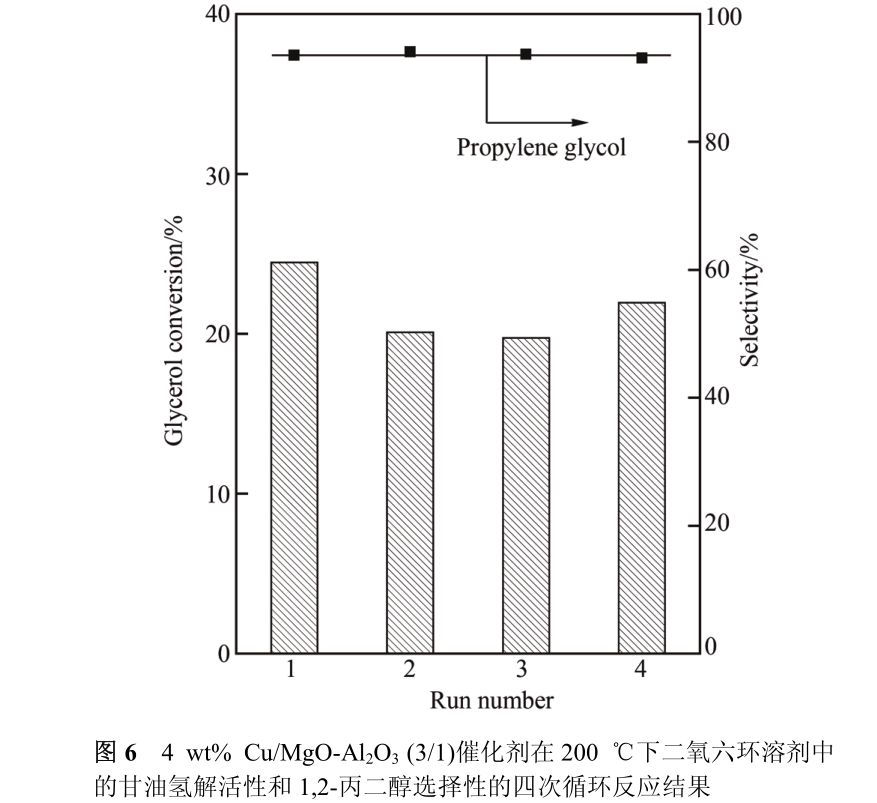
对 4 wt% Cu/MgO-Al 2 O 3 (3/1) 催化剂稳定性的考察结果表明, 在经过四次反应循环后, 催化剂的甘油氢解反应活性和选择性没有显著变化(图 6)。我们推测催化剂表面的羟基化在反应的初始阶段就已经发生,因此在催化剂表面上与 Mg 2+ 键连的羟基是催化剂上实际参与甘油氢解反应的碱性中心。
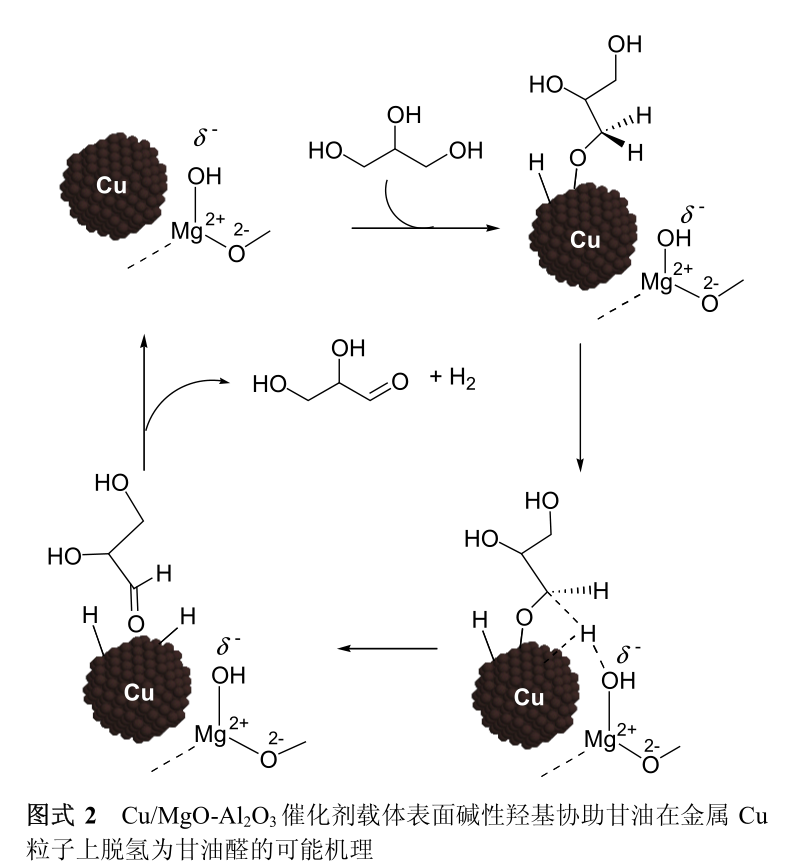
Cu/MgO-Al 2 O 3 催化剂表面碱性羟基协助金属Cu粒子完成甘油脱氢为甘油醛的可能机理如图式 2 所示: 首先,甘油分子在金属 Cu 表面解离吸附为醇氧基和氢原子。 醇氧基和在金属 Cu 与载体界面处的碱性羟基发生诱导极化作用使醇氧基的 α 位 C—H 键弱化。 得到弱化的醇氧基 α 位 C—H 键在金属 Cu 表面发生断裂并最终生成甘油醛和一分子 H 2 。